Трансплантация костного мозга (ТКМ) – это пересадка костного мозга от здорового донора к получателю, чей собственный костный мозг поражен болезнью. Трансплантация может быть использована для лечения апластической анемии; серповидно-клеточной анемии; различных злокачественных заболевании крови, в том числе лейкемии, множественной миеломы; некоторых твердых опухолей, таких как нейробластома; и заболеваний обмена веществ.
Содержание
- 1 История
- 2 Показания к трансплантации костного мозга
- 3 Что такое стволовые клетки
- 4 Трансплантация гемопоэтических стволовых клеток
- 5 Как стволовые клетки могут использоваться в медицине
- 6 При каких болезнях применяется операция по пересадке стволовых клеток
- 7 Пересадка костного мозга в России
- 8 Сколько стоит пересадка стволовых клеток
Сегодня тема стволовых клеток вышла далеко за пределы узких сугубо научных кругов. Об этих клетках часто можно услышать в научно-популярных источниках информации и даже в желтой прессе. В итоге реальные факты настолько перемешались с домыслами и явными сплетнями, что человеку, не искушенному в этом вопросе, порой трудно отделить плевел от пшеницы.
Из всего обилия информации складывается впечатление, что данный вид клеток – это чуть ли не панацея от всех болезней. Потенциальные возможности порой выдаются за реальные достижения, хотя в действительности до практического внедрения теоретически возможных технологий должен пройти не один десяток лет исследований. Стволовые клетки, подобно нанотехнологиям, сегодня стали мемом, активно используемым всеми кому ни лень в маркетинговых целях, для привлечения внимания потенциальных покупателей к некоему очередному чудо-продукту непонятного происхождения.
Что же в действительности представляют стволовые клетки, как их можно использовать на практике, и насколько возможности их применения реально реализованы в современной медицине?
История
Первая операция по пересадке костного мозга была передана пациенту с апластической анемией в 1939 году. Этот больной получал ежедневно переливание крови с целью поднять уровень лейкоцитов и тромбоцитов с помощью внутривенной инъекции костного мозга. После Второй мировой войны и использования атомной бомбы исследователи пытались найти способы восстановления функции костного мозга в аплазии, вызванной радиационным воздействием. В 1950-х годах было доказано на модели мыши, что аплазия костного мозга, вторичная по отношению к радиации, может быть преодолена с помощью трансплантата костного мозга. В 1956 году Барнс и его коллеги опубликовали свой эксперимент на двух группах мышей с острым лейкозом: обе группы были облучены как анти-лейкемической терапией и обе были спасены от аплазии костного мозга путем трансплантации костного мозга. В этих экспериментах были продемонстрированы три основных принципа аллогенной трансплантации стволовых клеток:
- роль препаративного антиолейкемического режима в ТГК
- способность новой приживленной иммунной системы предотвращать рецидив лейкоза
- активность приживленной иммунной системы по отношению к реципиенту.
В 1956 году американский врач Эдвард Донналл Томас осуществил первую успешную трансплантацию костного мозга между двумя людьми. Реципиент, больной лейкемией, принял гемопоэтические стволовые клетки от своего брата-близнеца – это позволило его организму сделать новые, здоровые клетки крови и иммунной системы. Томас разработал наркотики подавляющие иммунную систему, еще больше снижая шансы на отторжение трансплантата реципиентом. В 1969 году эти улучшения позволили Томасу провести первую успешную трансплантацию костного мозга у больного лейкемией, родственника, который не был идентичным близнецом. В 1990 году Эдвард Донналл Томас с американский хирург Джозефом Мюррэй были номинированы на Нобелевскую премию по физиологии или медицине за свою пионерскую работу по трансплантации костного мозга.
Показания к трансплантации костного мозга
Аутологичная гемопоэтическая трансплантация стволовых клеток (ауто-ТГСК) составляет 58% трансплантаций, сделанных в Европе; 47% ауто-ТГСК выполнены для лечения множественной миеломы, 30% для неходжкинской лимфомы, 11% для ходжкинской лимфомы и 3% для лейкемии. К другим менее распространенным показаниям для ауто-ТГСК относятся аутоиммунные заболевания (рассеянный склероз, системный склероз, болезнь Крона) и твердые опухоли (саркома, герминальные опухоли и нейробластома). Острый миелолейкоз и все они составляют 50% аллогенной ТГСК, миелодиспластический синдром и миелопролиферативные новообразования составляют 15%, а синдром недостаточности костного мозга – 6%. Более полный список показаний к пересадке костного мозга указан в таблице, она позволяет понять при каких заболеваниях необходима пересадка костного мозга.
Таблица 1. Современные показания для аутологичной и аллогенной трансплантации стволовых клеток
| Аутотрансплантация | Аллотрансплантация | |
| Злокачественности | Множественная миелома Неходжкинская лимфома Болезнь ходжкина Острый миелоидный лейкоз Нейробластома Рак яичников Опухоли зародышевых клеток | Острый миелоидный лейкоз Острый лимфобластный лейкоз Хронический миелолейкоз Миелодиспластический синдром Миелопролиферативные новообразования Неходжкинская лимфома |
| Незлокачественные расстройства | Аутоиммунное заболевание Амилоидоз | Апластическая анемия Пароксизмальная ночная гемоглобинурия Анемия Фанкони Анемия Даймонд-Блэкфан Талассемия Серповидноклеточная анемия Тяжелый комбинированный иммунодефицит Синдром Вискотта-Олдрича Врожденные ошибки метаболизма Врожденные нейтропенические синдромы |
Что такое стволовые клетки
Эти клетки являются недифференцированными предшественниками зрелых клеток различных тканей и органов. Зигота, образующаяся при оплодотворении яйцеклетки сперматозоидом и из которой развивается впоследствии все группы клеток эмбриона, также относится к стволовым.
Клетки этого типа имеют многие многоклеточные организмы. Особенностью стволовых клеток является то, что они способны трансформироваться в любые специализированные клетки. Именно за счет их происходит обновление органов и тканей в течение жизни.
Стволовые клетки составляют своего рода резервный фонд для организма человека или животного. С возрастом, однако, их запас постепенно уменьшается. Потому регенеративные процессы по мере старения протекают все с большим трудом.
Существуют различные группы стволовых клеток с тем или иным уровнем специализации, но всех им объединяют следующие свойства:
- способность к самообновлению – делению с образованием дочерних клеток, полностью идентичных материнским;
- способность к делению с образованием дочерних клеток, более специализированных, чем материнские.
Основные группы стволовых клеток
Стволовые клетки подразделяются на следующие группы:
- Эмбриональные клетки, составляющие клеточную массу зародыша на раннем этапе его развития. Характерной их особенностью является то, что они практически не отторгаются рецепиентом при пересадке их от донора, обладая почти идеальной приживаемостью. При трансплантации клеток этой группы животным с ослабленной иммунной системой появляются новообразования сложного строения, способные к злокачественному перерождению – тератомы. Поведение эмбриональных клеток в организме с полноценным иммунитетом пока что не изучено, но исследования в этом направлении уже начаты.
- Фетальные клетки, получаемые из плода, абортированного на девятой-двенадцатой неделе развития. Эта группа клеток характеризуется началом дифференциации – они делятся ограниченное число раз и трансформируются только в клетки конкретного органа или ткани.
- Постнатальные клетки, имеющиеся у зрелого организма. Эта группа клеток более дифференцирована, чем эмбриональные или фатальные клетки, потому обладает довольно ограниченной способностью к трансформации.
Постнатальные клетки сегодня наиболее применяемы на практике, так как их можно взять в лечебных целях у самого пациента. Потому использование этого материала не вызывает этических возражений. К тому же, возможность человека выступать в роли донора по отношению к самому себе делает лечение с использованием постнатальных клеток результативным и относительно безопасным.
Постнатальные клетки подразделяются на следующие разновидности:
- гемопоэтические клетки, дающие начало кровяным клеткам;
- мезенхимальные стромальные клетки, трансформирующиеся в костные, хрящевые и жировые клетки;
- прогениторные клетки, участвующие в процессе обновления тканей.
Трансплантация гемопоэтических стволовых клеток
Трансплантация гемопоэтических клеток – это узкоспециализированная и уникальная медицинская процедура. Аутологичная трансплантация позволяет проводить высокодозную химиотерапию без пролонгированной аплазии костного мозга. При аллогенной трансплантации стволовые клетки донорского происхождения обеспечивают аллоиммунный эффект, который позволяет устранить остаточные заболевания и предотвратить рецидив. Первая аллогенная трансплантация была проведена в 1957 году. С тех пор поле эволюционировало. Новые показания помимо острого лейкоза и апластической анемии постоянно изучаются и теперь включают врожденные нарушения кроветворной системы, нарушения обмена веществ и аутоиммунные заболевания. Использование неродственных доноров гемопоэтических стволовых клеток и частично родственных доноров значительно расширило доступность аллогенной трансплантации. Смертность, связанная с трансплантацией, снизилась благодаря улучшению поддерживающего ухода, включая более эффективные стратегии профилактики тяжелых инфекций, а также благодаря включению протоколов, которые снижают токсичность и допускают трансплантацию у пожилых пациентов. Тем не менее, рецидив заболевания и болезнь “трансплантат против хозяина” остаются двумя основными причинами смертности при неудовлетворительном прогрессе. Интенсивные исследования, направленные на улучшение адоптивной иммунотерапии и повышение реакции трансплантата на лейкемию, в то время как снижение реакции трансплантата на хозяина может принести следующий прорыв в аллогенной трансплантации. Уже доказана клиническая эффективность стратегий манипуляций с трансплантатом, вакцинаций с опухолевыми антигенами, моноклональными антителами и адоптивной клеточной иммунотерапией. В последующие годы аллогенная трансплантация, скорее всего, станет более сложной, индивидуализированной и эффективной.
Как стволовые клетки могут использоваться в медицине
Сегодня много говорят о возможностях применении стволовых клеток при решении тех или иных медицинских проблем. Оптимисты заявляют, что использование стволовых клеток позволяет создать любой орган буквально в пробирке, стирая тем самым грани между реальностью и научной фантастикой. Действительно, подобные опыты проводятся. Например, российским ученым удалось из стволовых клеток создать искусственную щитовидную железу мыши. Но широкое внедрение технологий выращивания органов в практику возможно лишь в отдаленном будущем.
Потенциально в медицине могут быть применены клетки всех трех типов. Каковы же возможности их использования?
Применение эмбриональных клеток
Каждая эмбриональная клетка может трансформироваться в любую специализированную клетку. Клетки этой группы являются универсальным строительным материалом для любых тканей. Эмбриональные клетки, при введении их в организм реципиента, способны самостоятельно найти дефекты органов и тканей и ликвидировать имеющиеся неполадки. Потому они могут быть использованы для искусственного омоложения. Однако практическое их применение встречает следующие проблемы.
- Поскольку в зрелом организме эти клетки отсутствуют, человек не может являться их донором для самого себя. Попытка взять эти клетки у человеческого эмбриона для дальнейшего сохранения и использования приведет к гибели зародыша.
- Использование в качестве источника клеточного материала человеческих эмбрионов является практикой, весьма спорной в этическом отношении, и встречает активное противостояние со стороны общественности и различных религиозных организаций.
- Взаимодействие донорского организма с чужеродными эмбриональными клетками еще мало изучено, и потому невозможно точно спрогнозировать последствия их введения.
Предполагается, что причиной смерти целого ряда известных актеров от раковых заболеваний стала попытка омолодиться с помощью эмбриональных клеток. Во-первых, донорский клеточный материал мог содержать клетки, претерпевшие злокачественную трансформацию. Во-вторых, возможно, введение чужеродной клеточной культуры вызвало повышенную нагрузку на иммунитет, что и спровоцировало развитие опухолей.
Перспективной темой для исследований является изучение возможности пересадки человеку эмбриональных клеток животных.
Применение фетальных клеток
Подобно эмбриональным, фетальные клетки служат строительным материалом для органов и тканей. Однако из произвольно взятой клетки этой группы может развиться не любая ткань, а только ткани, соответствующие изначальной природе данной клетки. Несмотря на риск отторжения и опасность инфицирования организма пациента патогенными микроорганизмами, возможно содержащимися в донорском материале, эта группа клеток сегодня применяется достаточно широко. Как и применение эмбриональных клеток, использование фатальных клеток вызывает неприятие со стороны консервативно настроенных людей, воспринимающих такие медицинские технологии как покушение на человеческую жизнь и возможность для развития преступного бизнеса.
Использование постнатальных клеток
Эта группа клеток сохраняется в организме человека после рождения. Потому становится возможным лечение пациента с помощью его же собственных клеток. Это исключает возможность отторжения трансплантата и автоматически снимает этическую проблематику. В человеческом организме имеются следующие источники постнатальных стволовых клеток для использования в лечебных целях:
- Костный мозг тазовой области. Из него могут быть при помощи пункции выделены стромальные клетки, способные превратиться, например, в нервную или сердечную мышечную ткань. Последнее делает их применимыми для восстановления сердца после инфаркта.
- Кровь, содержащаяся в пуповине. Эта кровь может быть собрана и заморожена, а стволовые клетки, в ней содержащиеся, могут быть впоследствии использованы в лечебных целей. Пуповинные стволовые клетки отличает высокий уровень универсальности: из них можно создать практически любую ткань.
- Плацента. Количество стволовых клеток в этом органе десятикратно превышает их содержание в пуповинной крови. Из плацентарных клеток могут развиться нейроны, а также клетки кожи, крови и мышц. Несмотря на высокую стоимость создания криобанка пуповинных и плацентарных клеток, их применение все более расширяется.
- Слизистая оболочка носоглотки. В ней содержаться стволовые клетки, способные породить нервную ткань.
- Жировая, хрящевая и мышечная ткань.
Постнатальные стволовые клетки обладают генетической меткой, указывающей на их принадлежность к конкретному организму. Потому они могут отторгаться при пересадке от одного человека к другому. Менее всего это свойство выражено у пуповинных клеток – отторжение их происходит только тогда, когда донор и реципиент несовместимы по антигенам.
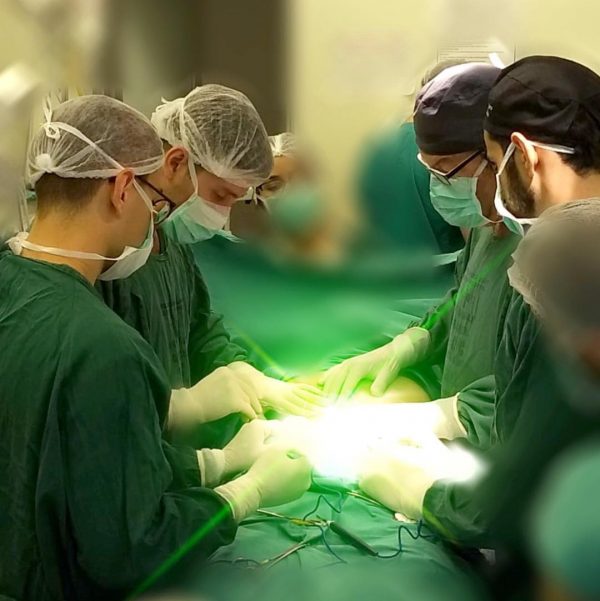
При каких болезнях применяется операция по пересадке стволовых клеток
Сегодня трансплантация стволовых клеток способна помочь при различных патологиях, включая даже те, которые прежде считались неизлечимыми. Введение этих клеток позволяет если и не вылечить больного полностью, то заметно улучшить его состояние. Данный метод лечения успешно применяется при лечении автоиммунных (рассеянный склероз) и онкологических (лейкоз) заболеваний, а также для ликвидации последствий инфарктов и инсультов.
Пересадка стволовых клеток при рассеянном склерозе
Рассеянный склероз – тяжелое аутоиммунное заболевание, характеризующееся прогрессирующим разрушением нервных волокон с последующей их заменой на соединительную ткань. Болезнь проявляется в нарушении координации движений, проблемах умственной деятельности, парезах. В тяжелых случаях развитие заболевания может привести к полному обездвиживанию.
Суть заболевания состоит в выработке клетками иммунной системы больного антител к миелину – веществу, входящему в состав нервных волокон. В результате организм человека, страдающего рассеянным склерозом, сам уничтожает свою же нервную ткань.
Пересадка костного мозга при рассеянном склерозе прежде рассматривалась как наиболее перспективный путь лечения заболевания. В настоящее время этот метод считается радикальным и применяется редко – только при отсутствии положительных результатов использования других способов терапии. Основная идея лечения рассеянного склероза данным методом заключается в замене прежних иммунных клеток на новые, которые не оказывают разрушающего действия на миелин. Для этого выполняются следующие шаги:
- Выделение стволовых клеток из предварительно отобранной крови.
- Многократное увеличение количества этих клеток путем клонирования.
- Уничтожение иммунных и кровеобразующих клеток у пациента посредством химиотерапии.
- Введение в организм больного стволовых клеток, которые заменяют убитые и не разрушают нервные волокна.
Этот способ сегодня применяют лишь в крайних случаях по следующим причинам:
- положительный результат такого лечения носит временный характер;
- разработаны новые, менее рискованные способы терапии при рассеянном склерозе;
- из-за уничтожения иммунных клеток возникает опасность появления злокачественных новообразований.
Пересадка стволовых клеток при лимфоме
Лимфома – онкологическое заболевание, поражающее лимфатические узлы. Сегодня эта болезнь эффективно лечится химиотерапией. Но в некоторых случаях для достижения положительного результата лечения нужны столь высокие дозы препаратов, что у пациента, прошедшего химиотерапию, имеет место тяжелое угнетение кровообразования. Необходимость применения обучения еще более усугубляет ситуацию. Для таких больных требуется трансплантация стволовых клеток, добываемых из крови или костного мозга их самих либо доноров.
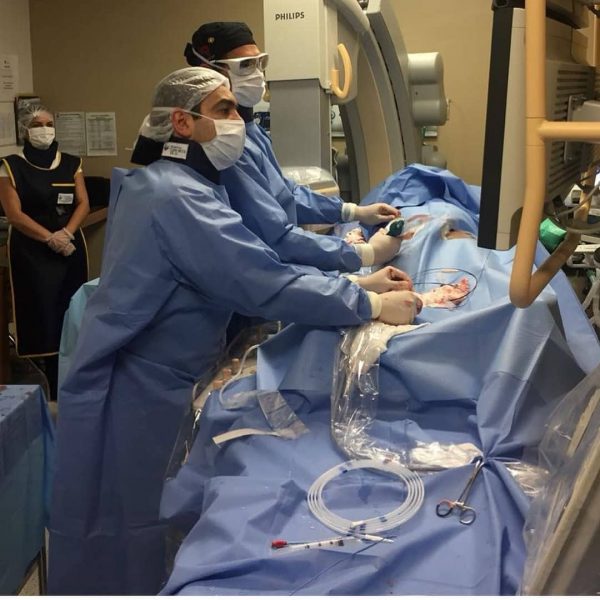
Предпочтительно, чтобы донор состоял в близком родстве с пациентом. В этом случае иммунная несовместимость наименее вероятна. Введение в организм пациента стволовых клеток приводит к постепенному восстановлению иммунитета и кровообразования. На это обычно требуется от двух недель до месяца.
Пересадка костного мозга при лимфоме Ходжкина
Аутологичная трансплантация стволовых клеток считается “золотым стандартом” после восстановительной химиотерапии при рецидивной или рефрактерной лимфоме Ходжкина. Первое рандомизированное исследование, сравнивающее обычную химиотерапию и аутотрансплантацию, было опубликовано в 1993 году. Сорок пациентов получили этопозид, цитарабин и мелфалан в качестве схемы кондиционирования. Результаты показали превосходство трансплантации. Европейская группа по трансплантации крови и костного мозга опубликовала подтверждающее рандомизированное исследование. При медианном наблюдении в течение 3 лет, выживаемость составила 55% против 34% для трансплантата и химиотерапии, соответственно. Трансплантация костного мозга при лимфоме Ходжкина все еще является экспериментальной процедурой и ее целесообразность изучается.
Пересадка костного мозга при неходжкинской лимфоме
Высокодозная миелоаблятивная терапия аутологичной или аллогенной стволовой клеткой является эффективной стратегией лечения неходжкинской лимфомы (НХЛ), но у НХЛ гораздо меньше шансов остаться в ремиссии после аутологичной трансплантации, чем после аллогенной трансплантации. Польза от проведения аутологичной трансплантации на более раннем этапе заболевания, особенно для пациентов, которые имеют промежуточные или высокие баллы по международному Прогностическому индексу факторов риска, по-прежнему остается неясной. Добавление иммунотерапии, биологических модификаторов и терапии антителами, такими как ритуксимаб или радиолабелированное антитело, к аутологичной трансплантации – это подходы, проходящие оценку. Исторически сложилось так, что был высокий уровень смертности, связанный с режимом, связанный с миелоаблятивной аллогенной трансплантацией, что сделало этот подход менее привлекательным для терапии. Использование невосприимчивых аллогенных трансплантатов в качестве лечения НХЛ изучено менее хорошо и находится на стадии рассмотрения.
Пересадка костного мозга при лейкозе
Лейкоз (лейкемия, рак крови, белокровье) характеризуется злокачественным перерождением как гемопоэтических, так и зрелых кровяных клеток. Для лечения лейкоза применяются химиотерапия и облучение, уничтожающие злокачественные клетки костного мозга. Побочным действием этих методов является уничтожение не только больных, но и здоровых клеток, ответственных за иммунитет и образование крови.
Для восстановления иммунитета и кроветворения применяется аутологичная или аллогенная трансплантация гемопоэтических стволовых клеток. В первом случае донором клеточного материала выступает сам больной, а во втором – человек, чьи ткани совместимы с тканями пациента.
Традиционно трансплантацию гемопоэтических клеток называют пересадкой костного мозга, хотя сегодня этот термин начинает терять свою актуальность. Классический способ получения стволовых клеток из костного мозга тазовых костей представляет собой длительную операцию, проводимую под общим обезболиванием в условиях стационара. В ходе этой процедуры делаются пункции костей таза, которые оставляют после себя болезненные ощущения. Пересадка костного мозга при лейкемии постепенно вытесняется взятием стволовых гемопоэтических клеток из периферической или пуповинной крови.
Введение гемопоэтических клеток пациенту приводит к восстановлению кроветворения и функций иммунной системы.
Лейкемия представляет собой наиболее распространенную детскую злокачественную опухоль, на которую приходится примерно 30% всех случаев рака у детей в возрасте до 20 лет. Большинство детей с диагнозом лейкемия излечиваются без пересадки стволовых клеток при лейкозе, но для некоторых подгрупп высокого риска аллогенная трансплантация играет важную роль в их терапевтическом подходе.
Аутологичная трансплантация костного мозга при лейкемии была разработана для расширения видимого лечебного потенциала миелоабляционной терапии аллогенной трансплантацией костного мозга лейкозным пациентам без гистокомпатных доноров костного мозга. Концептуальная проблема такого подхода очевидна: если необходимость трансплантации основана на явном или оккультном заражении костного мозга лейкемией, то использование аутологичного костного мозга, по-видимому, обречено на провал из-за реинфузии лейкозных клеток вместе с собранным костным мозгом.
Пересадка костного мозга в России
Ежегодно в России выполняется 50-60 аллотрансплантаций костного мозга, против 400-700 аналогичных операций в США или Европе. Низкое количество операций объясняется тем, что в стране недостаточно специализированных центров по выполнению подобных процедур.
ТКМ – это очень дорогая процедура, которая требует современного оборудования, применения дорогих зарубежных лекарственных средств и реагентов, подготовленного медицинского персонала. К сожалению, из-за ограниченного финансирования данная отрасль трансплантологии развивается в России очень медленно.
Где в России делают пересадку костного мозга
Первым центром предложившим такие услуги является НИИ ДОГиТ им. Р. М. Горбачевой (Санкт-Петербург). Данный научно-исследовательский институт является лидером в своей области.
Трансплантация костного мозга в России проводится также на базе других центров и клиник:
- Городская клиническая больница №31. Центр онкогематологии. Отделение трансплантации костного мозга. (Санкт-Петербург)
- Российская детская клиническая больница (РДКБ ФГБОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России) (Москва). На базе данного медицинского учреждения впервые в России в 1997 была сделана неродственная пересадка костного мозга ребенку 2-х лет.
- НМИЦ ДГОИ им. Дмитрия Рогачева (Москва)
- НМИЦ онкологии им. Н.Н. Блохина (Москва)
- ФГБУ «НМИЦ гематологии» Минздрава России (Москва)
- Свердловская областная клиническая больница №1 (Екатеринбург)
Сколько стоит пересадка костного мозга в России
Стоимость пересадки костного мозга в России колеблется в районе 1-3 миллионов рублей. Точная цена стоимости может быть рассчитана только после проведения тщательного обследования пациента и определения того, какой именно вид трансплантации будет необходим.
По этой причине не всегда можно определить заранее, где лучше, с финансовой точки зрения, проводить операцию – в России или в западных странах. Так как в мире существует общая Международная донорская база, клиники России, аналогично другим могут находить в ней подходящих доноров. В этом аспекте отечественные клиники имеют полный доступ ко всем данным.
Сколько стоит пересадка стволовых клеток
Лечение стволовыми клетками – дорогостоящая процедура, так как выращивание клеточной культуры и ее подготовка требуют применения высоких технологий. Цена трансплантации зависит от количества клеток, требуемых для лечения, которое может быть связано с возрастом пациента и другими факторами. Стоимость трансплантации возрастает в случае необходимости проведения хирургической операции. Аллогенная пересадка стоит дороже аутологичной. Если говорить конкретно о стоимости пересадки костного мозга, то цена на эту операцию лежит в диапазоне от нескольких десятков до нескольких сотен тысяч долларов. Наиболее дороги операции в американских клиниках (от 120 тысяч долларов), а наиболее дешевы – в Индии (от 30 тысяч долларов).