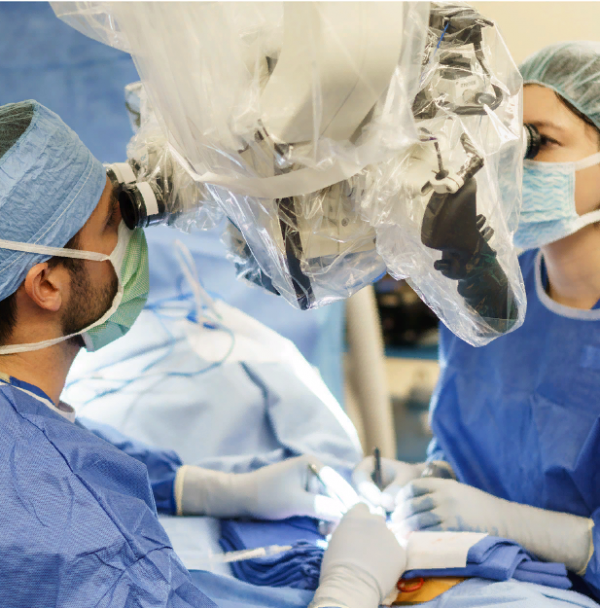
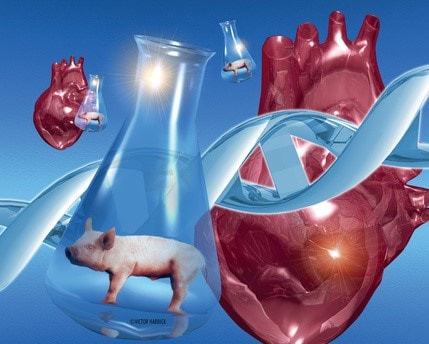
 Ксенотрансплантация (межвидовая трансплантация) открывает перспективу неограниченного предложения органов и клеток для клинической трансплантации, тем самым устраняя критическую нехватку тканей человека, которая в настоящее время создает большую очередь на получение трансплантатов. Животные трансплантации активно исследуются самыми передовыми научными центрами мира.
Ксенотрансплантация (межвидовая трансплантация) открывает перспективу неограниченного предложения органов и клеток для клинической трансплантации, тем самым устраняя критическую нехватку тканей человека, которая в настоящее время создает большую очередь на получение трансплантатов. Животные трансплантации активно исследуются самыми передовыми научными центрами мира.
Содержание
История ксенотрансплантации
Между 17-м и 20-м веками кровь переливалась из различных видов животных в пациентов с различными патологическими состояниями. Кожные трансплантаты были проведены в 19 веке из различных животных, причем лягушки были наиболее популярными. В 1920-х годах Воронов выступал за трансплантацию кусочков яичка шимпанзе пожилым мужчинам, “изюминка жизни” которых ухудшалась, полагая, что гормоны, вырабатываемые семенником, будут омолаживать его пациентов. Вслед за новаторской хирургической работой Карреля, разработавшего методику анастомоза кровеносных сосудов, в 20 веке были проведены многочисленные попытки трансплантации органов нечеловеческого примата у пациентов.
В 1963-1964 годах, когда органы человека не были доступны, а хронический диализ еще не использовался, Реемцма пересадил почки шимпандзе 13 пациентам, один из которых вернулся на работу в течение почти 9 месяцев, прежде чем внезапно умереть от того, что считалось нарушением электролита. Первая пересадка сердца у человека, когда-либо выполненная Харди в 1964 году, с использованием сердца шимпанзе, но пациент умер в течение 2 часов. Старзл провел первую трансплантацию печени шимпанзе – человеку в 1966 году; в 1992 году он получил выживание в течение 70 дней после трансплантации печени бабуина.
С появлением технологий генной инженерии и клонирования, свиньи в настоящее время доступны с рядом различных манипуляций, которые защищают свои ткани от иммунного ответа человека, что приводит к увеличению выживания трансплантата свиней в нечеловеческих приматных моделях. Генетически модифицированные свиньи дают надежду на неограниченный запас органов и клеток для тех, кто нуждается в трансплантации.
Растущий спрос на органы, ткани и клетки в целях клинической трансплантации, и относительное отсутствие повышения числа умерших человеческих органов, которые становятся доступными каждый год, повысился интерес к возможности использования органов и клеток животных. Концепция межвидовой трансплантации (или ксенотрансплантация) не нова, и было проведено удивительно большое количество клинических попыток трансплантаций в течение последних 300 лет. Барьеры на пути ксенотрансплантации значительны, но постоянно преодолеваются, в основном благодаря нашей способности генетически проектировать свиней, чтобы сделать их ткани более устойчивыми к иммунной реакции человека.
Ксенотрансплантация в мифологии

Обзор греческой мифологии и религиозных трактатов — особенно, индуистской религии – обращает внимание на тот факт, что люди были заинтересованы в возможности слияния физических особенностей различных видов животных в течение сотен лет. Например, химера была использована для представления аллотрансплантации органов и клеток (трансплантация между членами одного и того же вида), а Ламассу была выбрана в качестве мифологической фигуры для представления Международной Ассоциации Ксенотрансплантации и ее официального научного журнала, Ксенотрансплантация.
Покойный Кит Реемцма отметил, что, возможно, одним из самых ранних примеров ксенотрансплантации была попытка Дедала и его сына Икара летать через море от Крита до материковой Греции с помощью птичьих крыльев, прикрепленных к их рукам. Икар потерпел неудачу, а Реемцма описал это как возможный случай гиперострого отказа (очень быстрое отторжение трансплантата), хотя он считал, что это скорее связано с провалом термолабильного клея. Тем не менее, Дедал успешно совершил путешествие, обеспечив эту пару завидным 50%-ным успехом.
Ксенотрансфузия крови

Если мы смотрим за рамки мифологии и легенд, в 17 веке, Жан-Батист Дени начал клиническую практику переливания крови от животных к человеку Возможно, неудивительно, что результаты были неоднозначными. В результате ксенотрансфузия была запрещена во Франции на протяжении многих лет. Сегодня, с увеличением риска передачи инфекционных агентов с переливанием крови человека, можно было бы сделать пример для использования животного, такого как свинья (помещаемая под идеальные «чистые» условиях, чтобы гарантировать, что инфекционный агент не будет передан) в качестве источника клеток крови и продуктов крови в будущем. Фактически этот подход недавно был исследован несколькими группами.
Ксенотрансплантация роговицы
Примечательно, что в 1838 году была проведена первая ксенотрансплантация роговицы (от свиньи), тогда как первый роговичный аллотрансплантат (от человека к человеку) не пересаживался еще более 65 лет спустя, до 1905 года.
Проблемы ксенотрансплантации
- Физиология. Существует два вопроса с органами свиньи – это размер и долговечность. Сердце или почка молодой свиньи, когда они пригодны для пожертвования, могут по-прежнему иметь потенциал для быстрого роста; произойдет ли это, ученые не знают. Кроме того, естественная продолжительность жизни свиньи составляет лишь пятнадцать лет, и ничего не известно о старении в ксенотрансплантированных органах. Печень производит более двух тысяч белков, и ясно, что многие из них будут иметь несовместимую или отсутствующую функцию через видовой барьер. Это делает печеночную ксенотрансплантацию менее перспективной, чем других органов.
- Температура тела свиней составляет примерно 39 ° C, тогда как температура тела человека составляет около 37 ° C. Функциональные последствия этого для активности ферментов свиней при более низкой температуре остаются неясными.
- Гиперострое отторжение. До недавнего времени исследование фокусировалось на феномене ускоренного отторжения. Это характеризуется гистологически быстрым началом отеков, кровоизлиянием и сосудистым тромбозом, обусловлено наличием предварительно сформированных антител и происходит в течение нескольких минут после трансплантации.
- Микробиологический риск. Риск передачи инфекционных агентов через видовой барьер является серьезным беспокойством по поводу всего подхода к ксенотрансплантации. Многие такие агенты могут быть исключены из свиного стада с помощью скрупулезных методов земледелия. Такие методы включают стерилизацию как кормовой, так и питьевой воды и устранение всего белка млекопитающих из корма для предотвращения прионной инфекции. К сожалению, это не исключает риск передачи вирусов, чья ДНК интегрирована в ядро трансплантированных клеток, таких как эндогенные ретровирусы свиней (PERV). Невозможно доказать отрицательное – что новый патоген никогда не может быть перенесен от свиней человеку в результате ксенотрансплантации. И любое клиническое развитие ксенотрансплантации должно сопровождаться строгим и пожизненным микробиологическим мониторингом реципиентов.
Этические аспекты и проблемы
Этические аргументы, выраженные в отношении трансплантации от трансгенных животных к человеку, являются широкими и имеют различные диапазоны, основанные на их предмете и природе. Мнение этиков по этому вопросу разделилось. В первой группе этики считают, что сама природа такого действия неэтична и неприемлема независимо от последствий процедуры и ее последствий для человека или животных. Во второй группе процесс трансплантации считается неприемлемым, поскольку противоречивые результаты происходят как у людей, так и у животных.
Антропоцентрическая этика
Эта школа всегда была доминирующим видением в истории этики. Только человечество признано членом этического общества и основано на некоторых религиозных соображениях или некоторых выдающихся характеристиках, таких как интеллект, душа, речь и сложные коммуникации, человечество всегда находилось в центре внимания и саммита пирамиды этики, в то время как другие существа считаются уступающими человеку. В результате философы, которые поддерживают эту точку зрения, исследовали неприятные эффекты ксенотрансплантации от трансгенных животных только для «человека». С этой точки зрения возможные последствия, которые могут произойти с «человеческими существами», можно разделить на две группы «индивидуальные» и «коллективные».
- Индивидуальная человеческая (антропоцентрическая) критика. В индивидуальном измерении эффекты рассматриваются для «человека», получающего орган животного. Одним из наиболее важных вопросов является отсутствие достоверности и правильных научных данных о передаче вирусов и болезней от животных получателю. В результате жизни с животными или использования продуктов животного происхождения человечество заразилось некоторыми болезнями животных, такими как болезнь безумства коров или куриный грипп. Ожидается, что после трансплантации органов животных в организм человека, вероятность распространения вирусов и микроорганизмов также возрастает. Учитывая эту возможность, которая может легко поставить под угрозу благосостояние пациента, благополучие и даже жизнь, к сожалению, существует множество неопределенностей, которые врачи еще не смогли решить. Было доказано, что микроорганизмы живут в теле существа без каких-либо плохих последствий (так называемая: естественная микрофлора). Микрофлора видов может быть вредной и даже смертельной для других. С другой стороны, функции вирусов не являются полностью предсказуемыми, и они могут изменяться по своей природе из-за некоторой реакции прыжка; поэтому он может иметь необратимые последствия для нового хоста. Например, тип вируса простого герпеса (ВПГ) живет как естественная флора и безвреден в теле обезьяны паука, но когда он переносится в организм других видов, он вызывает лимфому или другие виды рака крови.
- Коллективная человеческая критика. Как было сказано ранее, диапазон возможных побочных эффектов этого процесса не ограничивается только получателем, а также оказывает влияние на родственников и общество. От родственников получателя есть возможность передачи вируса или болезнетворных факторов, супругам или сексуальному партнеру. Следовательно, они также должны быть проинформированы о процессе трансплантации и ее побочных эффектах. Здесь предлагается новая форма информированного согласия, в которой адресату задают вопрос не только пациента, но и некоторых людей, которые находятся в тесном контакте с получателем. В случае возникновения и распространения некоторых инфекционных заболеваний в обществе, особенно в эпидемиях, многие люди будут участвовать. Поэтому некоторые критики рассматривают трансплантацию трансгенных животных человеку против политики здравоохранения, которая направлена на то, чтобы сохранить большинство членов общества здоровыми. Таким образом, преимущества пациента-реципиента конфликтуют с обществом. Хотя до сих пор нет точного предела, человек может подвергнуть опасности другие выгоды для достижения своей. Кроме того, если ксенотрансплантация в организм человека принимается, органы тела будут рассматриваться как свойства для продажи и покупки. Наряду с этим альтруистическое пожертвование постепенно исчезнет из царства ценностей.
Этика на основе животных
Хотя в истории философии, из-за господства ориентированных на человека школ мысли, животные не считались непосредственно предметом этических соображений, но с помощью идей Джереми Бентама, основателя школы утилитаризма, животные были введенные в качестве жителей этического общества. Вопреки тому, что Кант думал о рациональности как единственном факторе, являющемся членом морального сообщества, Бентам считал, что разумность, способность чувствовать боль и удовольствие, или положительный или отрицательный опыт достаточно для того, чтобы иметь моральный статус.
Поскольку животные разумны, их можно считать субъектом этики. После него многие философы разделили моральный статус животных на две группы. Последователи прав животных считают их держателями прав, и их следует рассматривать как и аналогичные интересы человека. С другой стороны, сторонники благополучия животных полагали, что человек имеет право использовать животных для удовлетворения своих потребностей, если животное страдает и затраты на использование меньше, чем выгоды для людей.
Последняя школа более приветствуется во многих аспектах. Что касается использования органов животного в трансплантации в человека, некоторые из сторонников прав животных, таких как Том Риган, категорически не соглашались с тем, что люди используют животных для любых потребностей, подчеркивая равные права животных и человека. В результате, с их точки зрения, пытки и убийства животных, чтобы пересадить их органы людям, неэтичны и означают снижение статуса животных на вещи или на ящик для инструментов.
Наряду с этой точкой зрения другая группа философов по этике животных, особенно утилитарных философов, таких как Питер Сингер, не отказалась от идеи использовать животных для спасения человеческой жизни, и, напротив, только с помощью требований атрибуции они пытались ограничить и уменьшить количество и качество такого использования. С их точки зрения, в соответствии с обоснованной потребностью или необходимостью, и если выгоды преодолевают степень боли и страдания животных, их можно использовать для удовлетворения потребностей человека при правильном их лечении.
Однако эта группа считает, что межвидовая трансплантация также подвергается критике, поскольку она противоречит концепции благосостояния животных.
Что касается этой концепции, то были даны два определения. В широком определении животных следует держать в безопасности от некоторых негативных факторов, таких как жажда, голод, боль, страдания и психологическая напряженность.
Следовательно, учитывая вышеупомянутые факты, можно сделать вывод, что в нынешней ситуации ксенотрансплантация не является биоэтически оправданной; поэтому этот вопрос необходимо развивать дальше.
Вывод
Несмотря на то, что был достигнут прогресс в преодолении начального барьера гиперострого отторжения посредством модуляции локального иммунного ответа, теперь приходится иметь дело с другими аспектами иммунной системы. Текущая работа в основном направлена на производство трансгенных и нокаутных свиней. Наряду с этим – захватывающая возможность вызывать толерантность через смешанный гематопоэтический химеризм.
Тревога по поводу риска заражения может быть уменьшена данными, подтверждающими отсутствие передачи в хорошо контролируемых экспериментах, или путем идентификации штаммов свиней, неспособных передавать PERV. Тем не менее, всегда будут опасения, что эксперименты не позволили исключить передачу патогенов с очень большим временем задержки. Ксенотрансплантация действительно предлагает способ исключить дефицит в органах, доступных для трансплантации, хотя результаты могут быть хуже, чем результаты аллотрансплантации: большая иммунологическая несовместимость, с необходимостью более сильной иммунотерапии, может означать более низкую продолжительность жизни и более короткую выживаемость трансплантата. Против всех этих проблем ксенотрансплантация дает возможность сделать доступными функциональные твердые органы, при попадании, пациентам, у которых в настоящее время практически нет шансов получить трансплантацию.